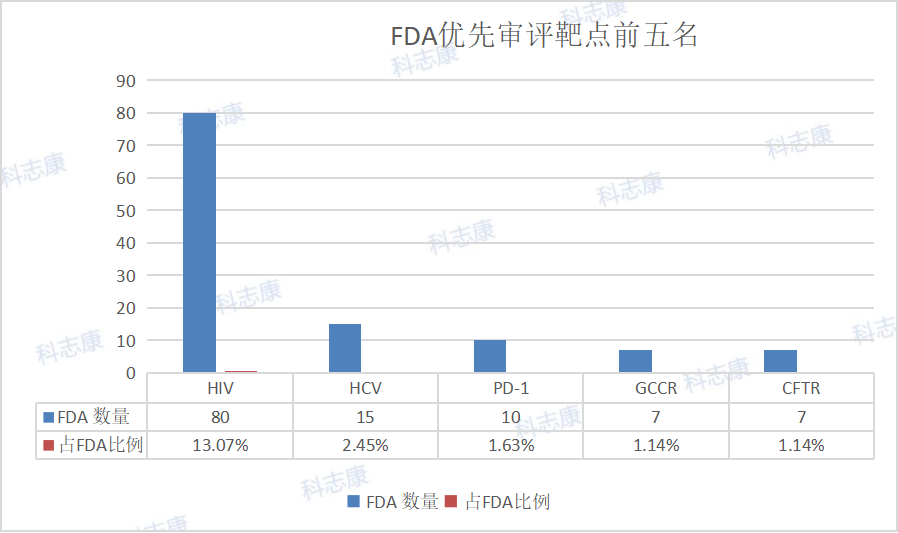
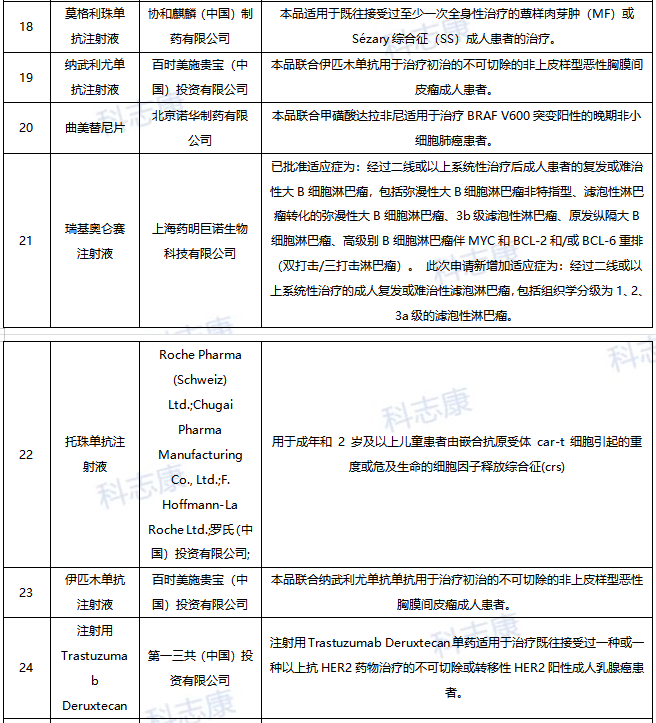
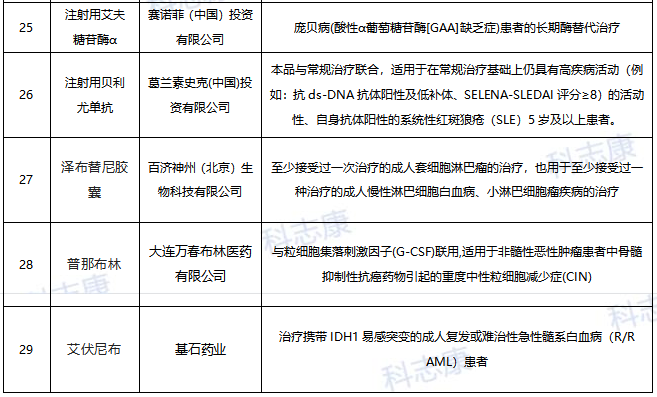
历年中美“优先审评”审批汇总对比分析

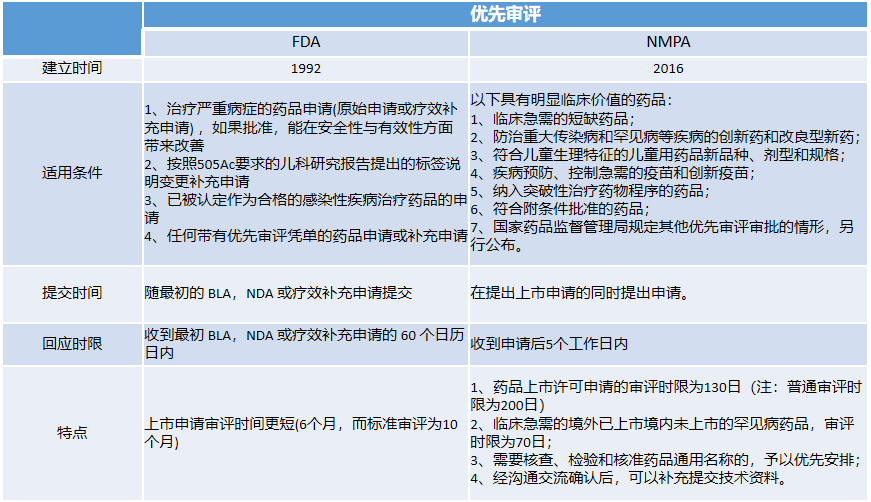
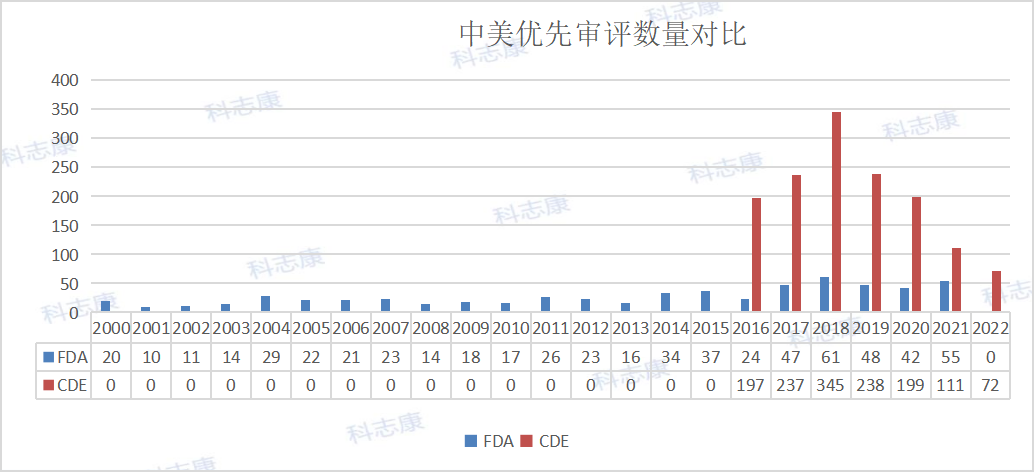
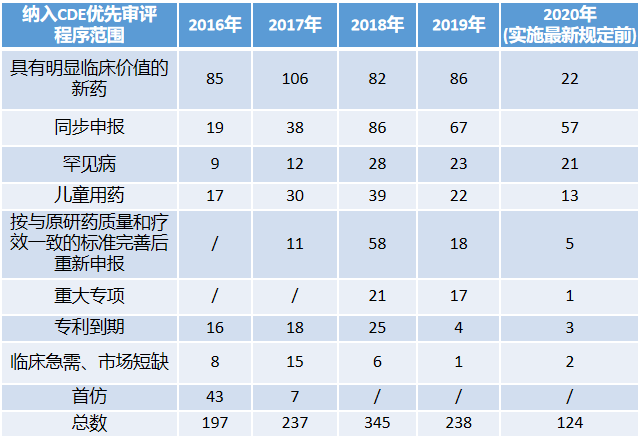
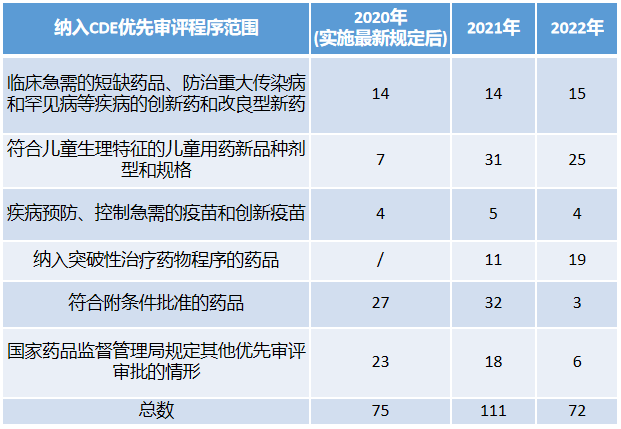
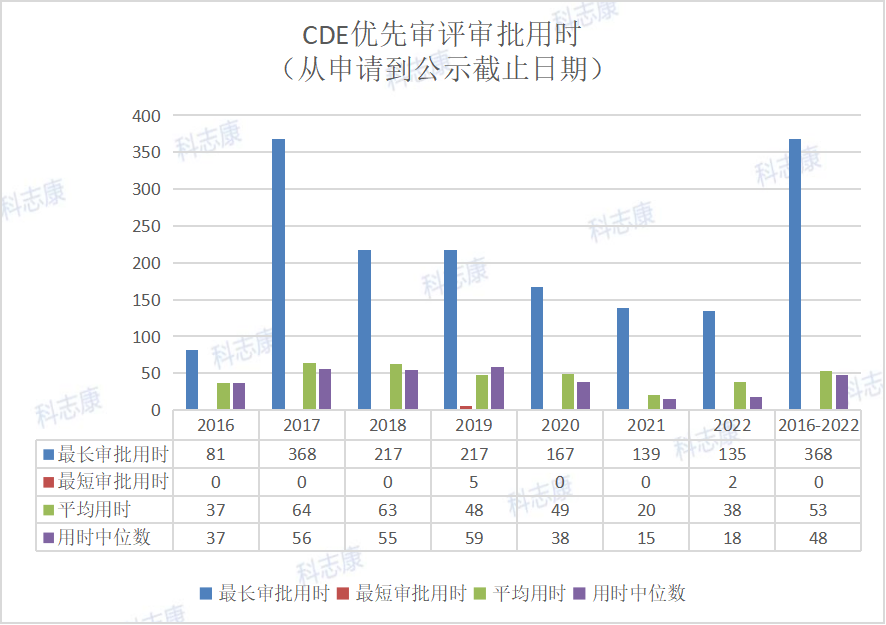
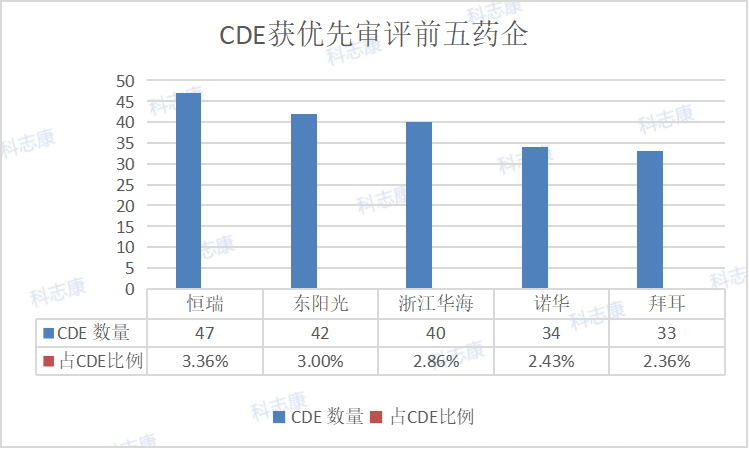
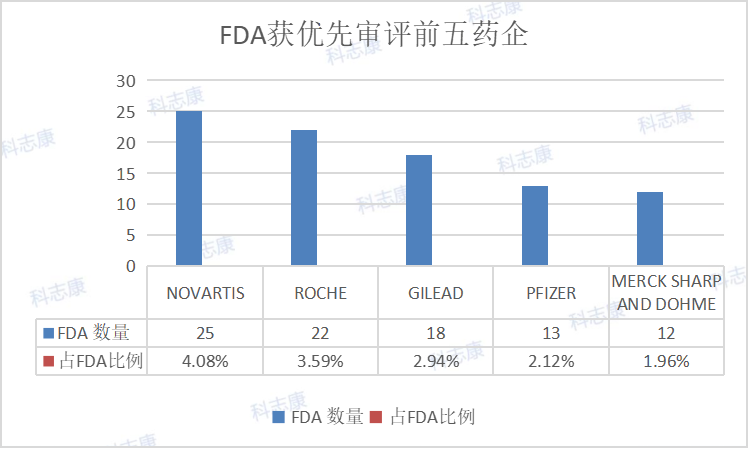
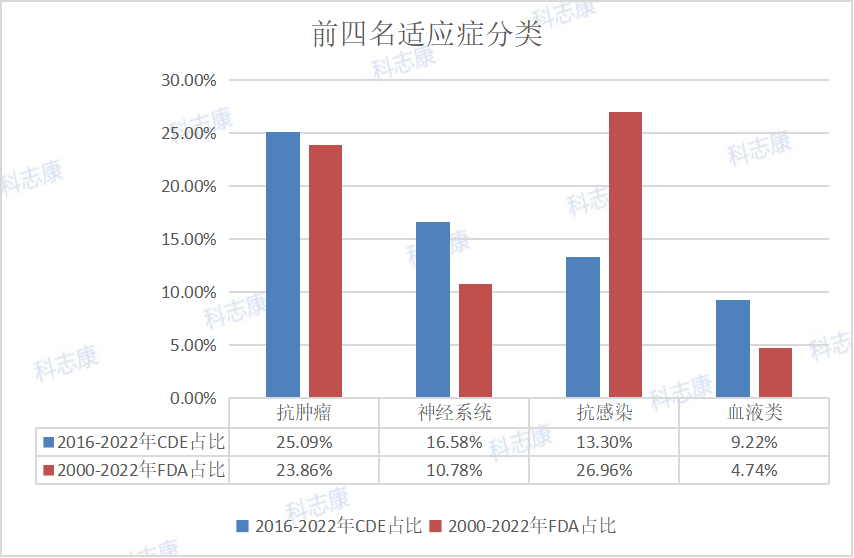
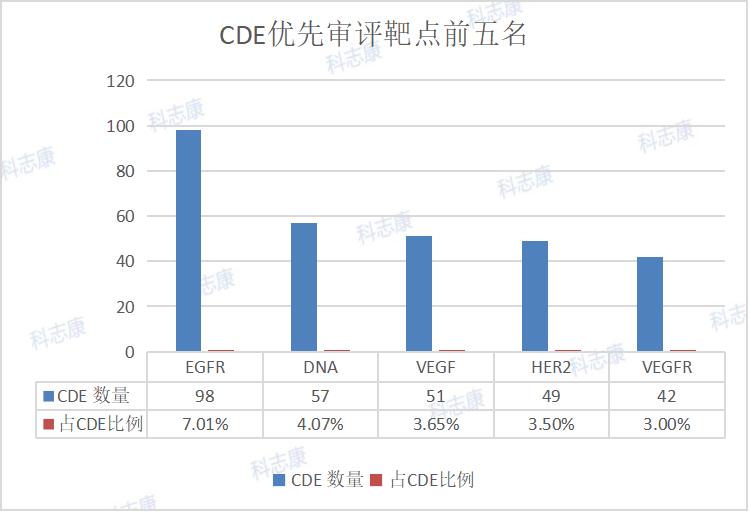
而以美国来看,有80个品种治疗HIV为最热门,HIV至今仍是未能治愈的疾病。排第二位的是HCV,治疗丙肝。PD-1对抗肿瘤、抗感染、抗自身免疫性疾病及器官移植存活等均有重要的意义。GCCR为炙手可热的血糖调节分子,带来糖尿病新疗法。CFTR则是治疗肺纤维化的实力靶点。
但是获得优先审评认证的药品上市也不一定可以一帆风顺。2011年在加速审批途径下,已获优先审评和孤儿药认证的Makena曾被FDA批准用于降低有自发性早产史的孕妇的早产风险。但是在今年4月6日,FDA宣布撤销对Makena的上市批准,因为在其规模更为庞大的验证性研究中,Makena没有显示临床益处。上市12年后遭撤市,这给了我们一个启示:药企应落实以临床价值为导向,以患者为核心的研发理念。唯有有明显临床价值的药品才可立足于市场,不断填补医疗需求空白。
历史文章:
强生IL-23抑制剂「古塞奇尤单抗」获CDE突破性疗法,治疗克罗恩病
被FDA和CDE纳入“突破疗法”和“优先审评”的普那布林能获批吗?
END


扫码关注
科志康

关于科志康


上海科志康医药科技有限公司,成立于2016年,是一家以药品监管科学为特色的研发咨询公司,致力于为客户定制法规解决方案,减少和避免在注册申报时“少做、漏做、重做、多做”的风险。
在药品注册时,公司提供高品质的一站式注册申报和模拟现场检查服务,为客户提高药品注册成功率。在研发过程中,公司提供第三方项目管理服务,法规前置,过程管理,协助制药企业提升药品研发效率。
目前,公司已与国内外79个知名制药企业建立合作,取得了100多项IND/NDA/ANDA佳绩。
公司使命:为制药企业提供专家解决方案,提升药品全生命周期合规性
公司愿景:助力制药企业研发和生产,让老百姓吃上放心药







